05/06/2019
難治性てんかん、ドラベ症候群とレノックス・ガストー症候群への有用性が認められているTHC、CBD製剤「エピディオレックス」が好調なGWファーマ(GW Pharmaceuticals plc, NASDAQ:GWPH)が、2019年3月末に締めた第1四半期決算を発表した。
<決算および事業ハイライト>
・ダレン・クラインがアメリカ市場のCEOに就任
・第1四半期のエピディオレックスの売上は、36.8億円($33.5M)。
・発売以来7600人の患者がエピディオレックスを処方される
・1900人以上の療法士がエピディオレックスを含む処方箋を発行
・医療保険(薬局)ネットワークは145のネットワーク拠点を構築
・拡張されたアクセスプログラムとオープンラベルでの処方を受けている900人の患者の約75%が商業製品への移行を完了。 残りの患者は、第2四半期末までに移行する見込み。
・米国での医療保険に関して、米国在住者の約90パーセント以上を現在カバーしており、そのうちの65パーセントは適応症のあることが事前承認(PA)されているか、処方箋を取得するハードルが容易な状況。
・医療保険のUnited HealthCare、OptumRx、およびPrime Therapeuticsは、エピディオレックスをカバーすることを決定。
・州がカバーするメディケイド加入者(米国の公的医療保険)99%のうち67%は補償範囲でカバーされるか、事前承認(PA)されているため処方箋を取得するのにハードルが厳しくない状況。
・7州では、制限なしでエピディオレックスが保険適用される。
・マネージド・メディケイド加入者(米国の公的医療保険)90%のうち40%は補償範囲でカバーされるか、事前承認(PA)されているため処方箋を取得するのにハードルが厳しくない状況。
・これまでに、レベル3と4のてんかんセンターを含む5,000人以上のヘルスケア専門家、約70%と関係性を構築。
・ヨーロッパの規制と発売前の進捗として、CHMPの見解は2019年半ばに発表となる予定。
・2019年末までにヨーロッパの主要5市場で発売予定。
・製造に関して、米国とヨーロッパの両方で予想される需要を満たすのに十分な生産能力を確保。
・臨床試験として、結節性硬化症複合体における第3相試験でプラセボと比較してエピディオレックスの良好な効果が認められた。
・アメリカFDAによる独占使用権は7年間となり、ヨーロッパでは10年間の独占権が認められている。
・てんかん治療においてCBD投与に関する知財をUSPIO(アメリカ特許庁)より取得。
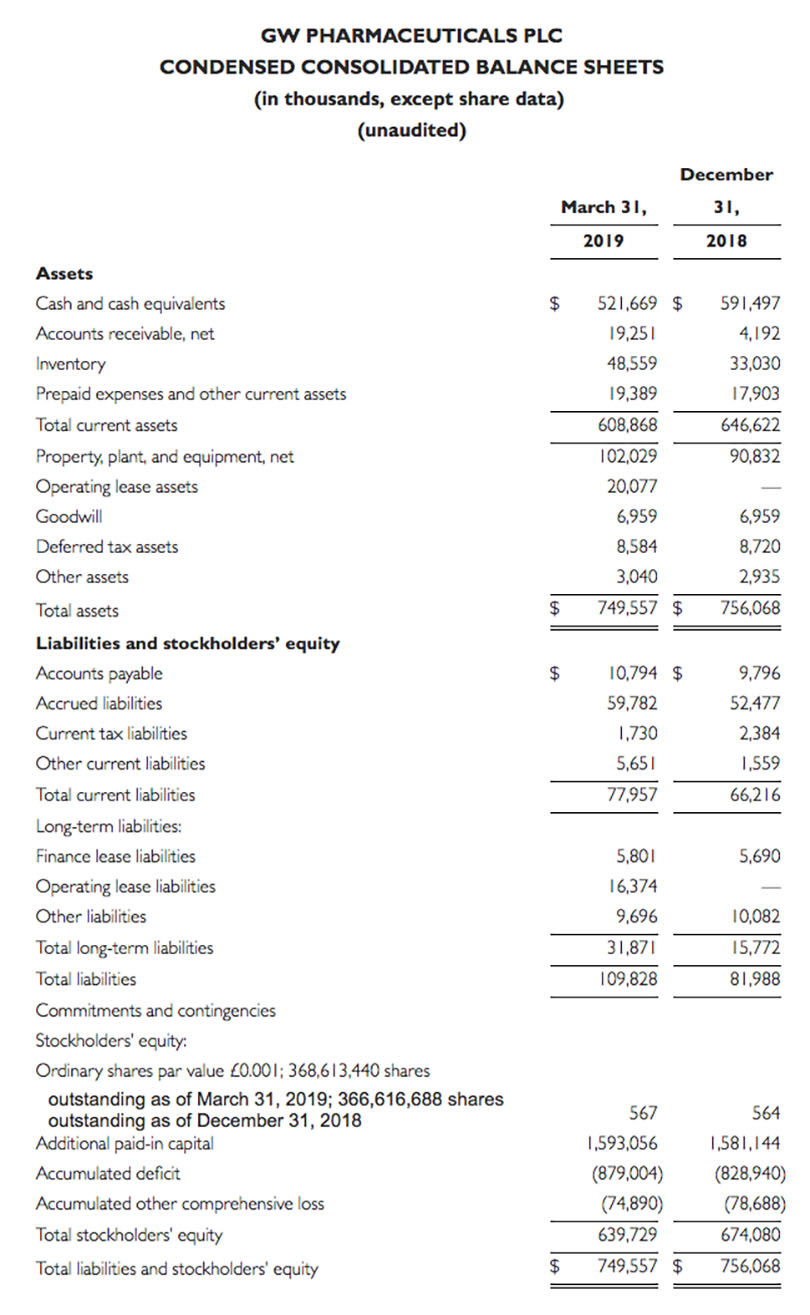
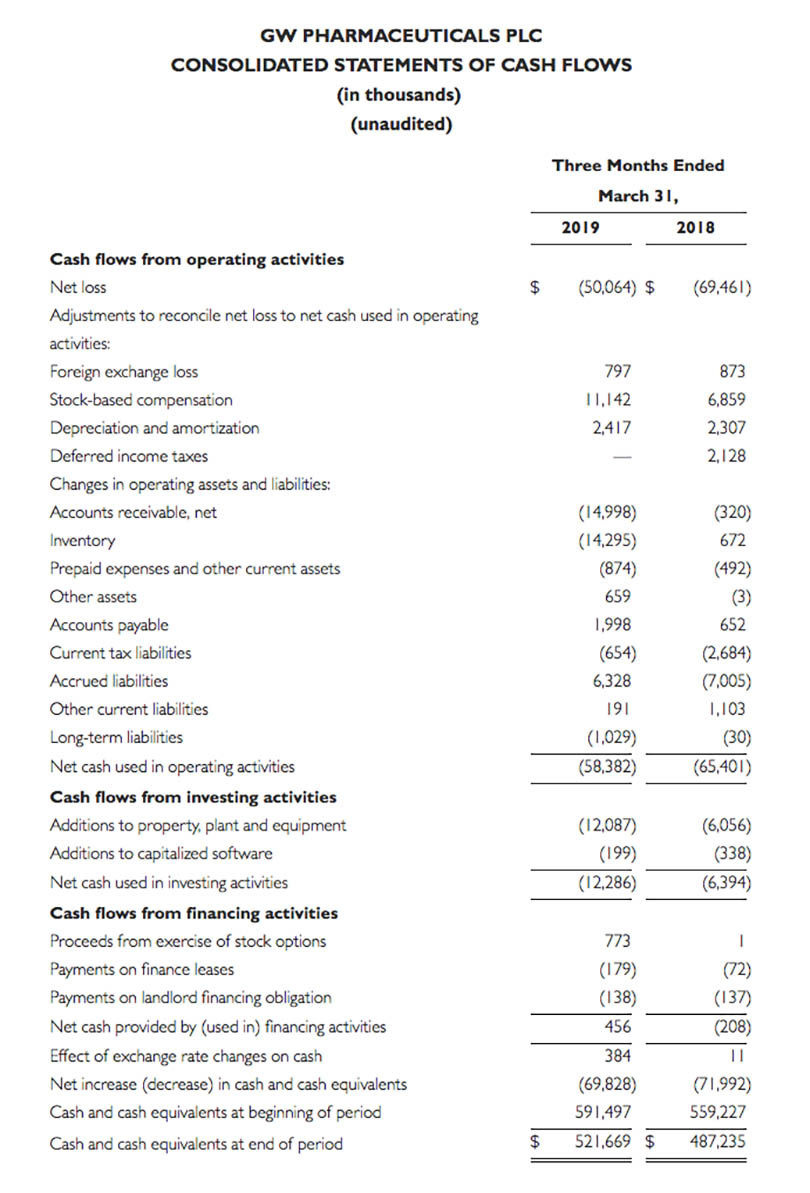
・2019年3月31日現在の現金および現金同等物は573.8億円($521.7M)、前年同期は650.6億円($591.5)。
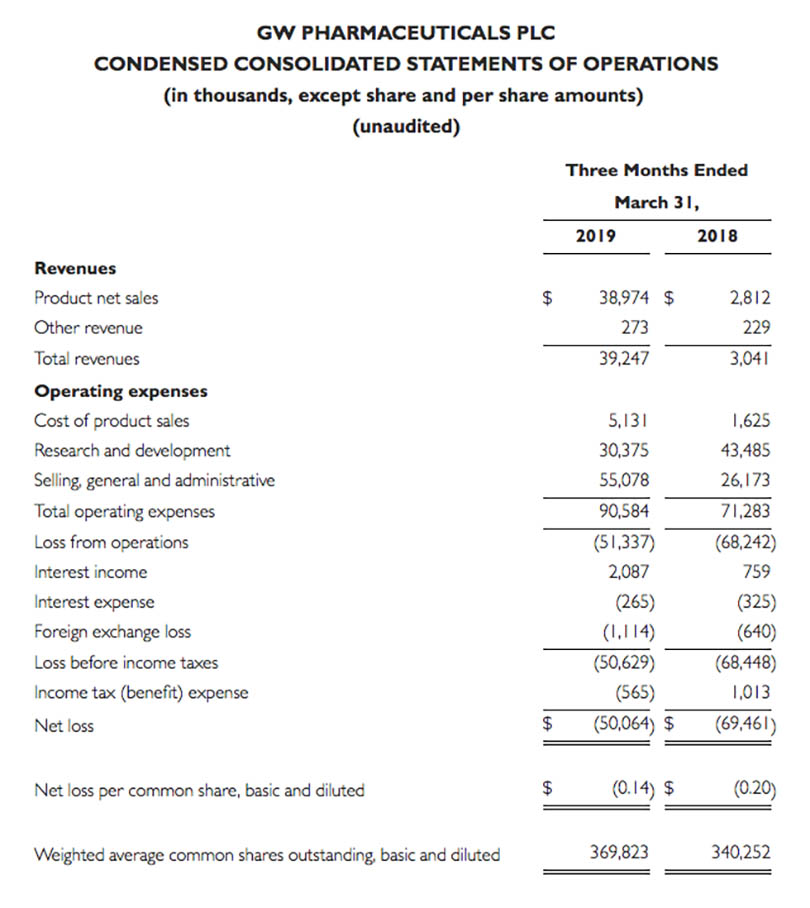
・2019年3月末四半期の売上は43.1億円($39.2)、前年同期3.3億円($3M)。
・2019年3月末四半期の純損失は55.1億円($50.1M)、前年同期76.4億円($69.5M)。
・2019年4月5日に希少小児疾病優先レビュー引換券を115億円($105M)で売却完了。この売却は2019年第2四半期の業績に反映される予定。
詳しくはGWファーマのプレスリリースをご参照ください。
—————————
<<新刊発売のお知らせ>>
「投資に役立つ!よくわかる大麻ビジネス」980円
カンナビストック・ジェーピー編集部 著
「ダメ!絶対!」が浸透している日本では考えられないことだが、アメリカ、カナダ、ヨーロッパで多くの企業がこの産業に参入し、彼らの多くはすでに大麻合法化へと向かう時代の流れを掴み、着々と事業を拡大している。
本書では、大麻ビジネスが世界でどのように展開されているのか、市場規模や各国の状況、そしてどのような産業や企業があるのかをざっと理解できるように構成している。
本書で取り上げた企業はほんの一部に過ぎないが、今後の大麻産業の流れを見る中でも押さえておきたい企業を取り上げた。
本サイトと合わせて読んでいただければ、大麻産業の”今”が理解できるでしょう。
—————————

